차세대 세포 치료제 제조를 위한 종합 솔루션
세포 치료제(Cell Therapy)는 환자 맞춤형 치료를 가능하게 하는 차세대 치료제로, CAR‑T를 시작으로 NK/CAR-NK, γδ T, TIL 등 다양한 형태로 빠르게 발전하고 있습니다. 하지만 이러한 세포 치료제 제조 공정은 작은 공정의 차이로도 최종 결과에 큰 영향을 줄 수 있습니다.
Cytiva는 세포 분리, 배양, 확장, 회수, 동결 보존에 이르기까지 세포 치료제 전 공정을 하나의 흐름으로 연결하는 End‑to‑End 솔루션을 제공합니다. 이를 통해 연구 및 공정 개발 단계부터 임상, 상업 생산 단계까지 이어지는 제조 공정을 보다 체계적이고 효율적으로 구축할 수 있도록 지원합니다.
통합 솔루션 확인Cytiva는 세포 분리, 배양, 확장, 회수, 동결 보존에 이르기까지 세포 치료제 전 공정을 하나의 흐름으로 연결하는 End‑to‑End 솔루션을 제공합니다. 이를 통해 연구 및 공정 개발 단계부터 임상, 상업 생산 단계까지 이어지는 제조 공정을 보다 체계적이고 효율적으로 구축할 수 있도록 지원합니다.

세포 치료제 제조 공정을
단순하게 만드는 공정 자동화
세포 치료제 제조는 높은 수작업 의존도와 공정 단계별 변동성이라는 구조적인 과제를 안고 있습니다. 특히 세포 분리, 활성화, 유전자 도입, 배양 및 확장과 같은 핵심 공정은 작업자 개입이 많을수록 공정 결과의 일관성 확보에 어려움이 발생할 수 있습니다.
Cytiva는 Cell Therapy 제조에 특화된 자동화 기반, closed system 플랫폼을 통해 CAR‑T 제조 공정의 표준화와 공정 재현성 확보를 지원합니다. 모듈형 설계를 기반으로 한 이 플랫폼은 연구 및 임상 단계에서 시작해 향후 상업 생산까지 확장 가능한 제조 전략 수립을 가능하게 합니다.
Cytiva는 Cell Therapy 제조에 특화된 자동화 기반, closed system 플랫폼을 통해 CAR‑T 제조 공정의 표준화와 공정 재현성 확보를 지원합니다. 모듈형 설계를 기반으로 한 이 플랫폼은 연구 및 임상 단계에서 시작해 향후 상업 생산까지 확장 가능한 제조 전략 수립을 가능하게 합니다.

디지털 기반 제조 관리와
cGMP 대응을 고려한 제조 환경
세포 치료제 제조 공정은 다수의 공정 변수와 대량의 데이터를 동반하며,이러한 정보를 체계적으로 관리하는 것은 공정 품질과 일관성 확보의 핵심 요소입니다. 특히 임상 및 상업 생산 단계로 진입할수록,제조 기록과 공정 이력 관리, 편차 대응은cGMP 요구사항과 밀접하게 연결됩니다.
Cytiva는 전자 배치 기록(Electronic Batch Record), eSOP 기반 작업 흐름, 공정 데이터 통합 관리를 포함한 디지털 기반 Cell Therapy 제조 환경을 제공하여, 공정 투명성과 추적성을 강화하고 cGMP 대응을 고려한 제조 운영을 지원합니다. 이를 통해 고객은 공정 관리 부담을 줄이고 보다 안정적인 세포 치료제 제조 환경을 구축할 수 있습니다.
Cytiva는 전자 배치 기록(Electronic Batch Record), eSOP 기반 작업 흐름, 공정 데이터 통합 관리를 포함한 디지털 기반 Cell Therapy 제조 환경을 제공하여, 공정 투명성과 추적성을 강화하고 cGMP 대응을 고려한 제조 운영을 지원합니다. 이를 통해 고객은 공정 관리 부담을 줄이고 보다 안정적인 세포 치료제 제조 환경을 구축할 수 있습니다.
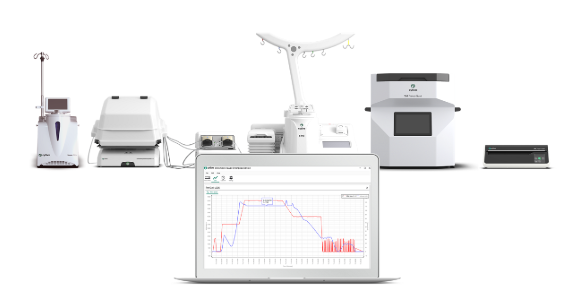
세포치료제 개발 전문성을 바탕으로 한
End‑to‑End 전문 지원 서비스
Cytiva는 세포 치료제 제조 환경에 대한 깊은 이해와 공정 전반에 걸쳐 축적된 경험을 바탕으로, 연구 단계부터 임상 및 상업 생산까지 이어지는 Cell Therapy 제조 워크플로를 지원합니다.
연구부터 GMP 생산까지, 사용 중인 장비와 소모품, 소프트웨어를 연계한 공정 개발 전략으로 세포 치료제 개발 전 과정을 효율적으로 지원합니다.
자세히 보기연구부터 GMP 생산까지, 사용 중인 장비와 소모품, 소프트웨어를 연계한 공정 개발 전략으로 세포 치료제 개발 전 과정을 효율적으로 지원합니다.

Cell therapy systems
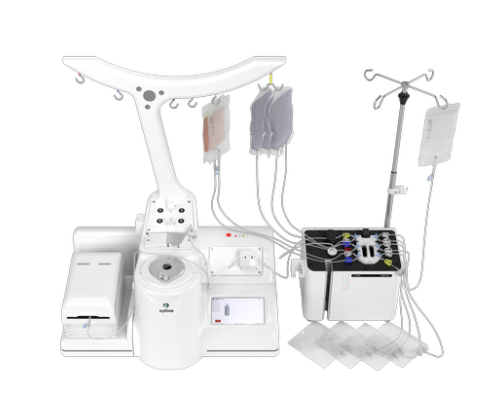
Sefia Select™ system
- 세포 분리, 세척, 제형화 단계를 통합한 자동화 시스템
- Closed system 설계로 오염 및 배치 리스크 최소화
- 다양한 애플리케이션과 사용자 정의 파라미터로 유연한 공정 대응
- Chronicle™ 연동 eBMR 및 실시간 모니터링, 21 CFR Part 11 지원

Sefia™ expansion system
- 세포 활성화, 유전자 도입 및 세포 배양 자동화 시스템
- 최대 1200 g 확장된 세포 수확 지원
- Chronicle™ 연동 Batch, Fed-batch, Perfusion 방식으로 확장 및 기존 시약, 배지와 호환 가능
- eBMR 및 실시간 모니터링, 21 CFR Part 11 지원

Sepax™ C-Pro
- 세포 세척 및 농축에 적합한 closed 원심분리 기술 사용 시스템
- 최대 1.2 L의 세포 용액을 최소 8 mL까지 농축 가능
- 연속 자동화 처리를 통해 사용자 작업 시간 단축 및 재현성 향상
- cGMP 요구사항 충족 및 IQ/OQ 지원 옵션 제공

VIA Freeze™
- LN₂ free 세포 동결 시스템
- 전도 방식의 냉각을 통한 균일한 냉각 기능을 제공하여 품질 편차 최소화
- 최적화된 동결 프로필을 저장 및 모든 샘플의 동결 과정 표준화 가능
- cGMP 요구사항 충족 및 FDA 21 CFR Part 11 준수. IQ/OQ 지원 옵션 제공

- Dry heat 기반 자동화된 세포 해동 시스템
- IR 센서를 통한 최적의 해동 프로세스를 자동으로 수행하여 해동 절차 표준화
- 다양한 bag 사이즈(10–275 mL) 동일 공정 적용
- cGMP 요구사항 충족, IQ/OQ 지원 옵션 제공
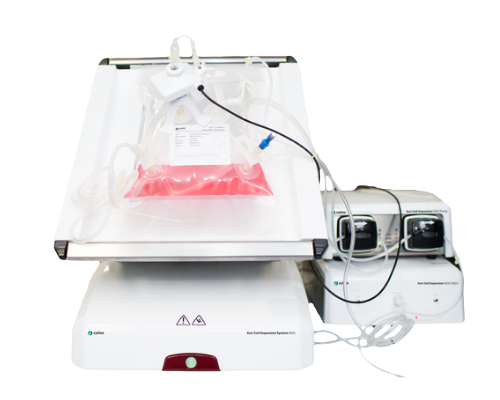
- 최대 25 L 규모의 세포 배양 환경 제공
- Perfusion 배양으로 고밀도 세포 배양 가능
- UNICORN™ 소프트웨어 기반 원격 모니터링 및 규제 환경 지원
- FDA 21 CFR Part 11 준수, IQ/OQ 지원 옵션 제공
Cell therapy media
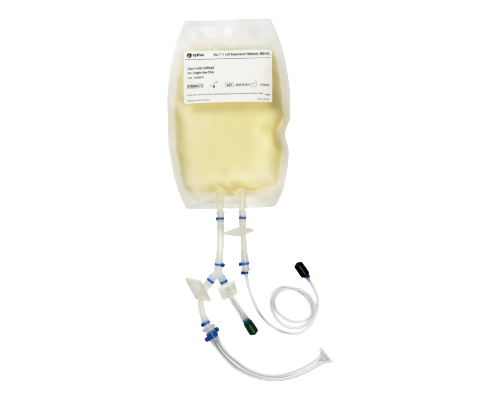
Xuri™ T cell expansion medium
- 인간 T세포 배양용 배지
- 동물 유래 성분 무첨가
- 배치 간 변동이 적은 일관된 품질 제공으로 공정 제어 향상
- USP <1043> 규정 준수

Ficoll-Paque™ PLUS
- 인간 림프구 분리용 배지
- 최대 1.078 g/ml 밀도 구현
- 높은 회수율과 B·T 세포 비율 유지
- Low endotoxin (< 0.12 EU/mL)

Ficoll-Paque™ PREMIUM
- 인간 림프구 분리용 배지
- ISO 13485 준수 및 QMS 기반 제조
- Low endotoxin(< 0.12 EU/mL) · Cytotoxicity grade 0
- 다양한 밀도 옵션(1.077 / 1.084 / 1.073 g/mL)
- Regulatory Support File(RSF) 제공

Ficoll™ PM 70
- Dextran‑sensitive 동물 대상 연구용 배지
- 평균 MW 70 000의 안정적인 sucrose 폴리머
- 낮은 독성 및 우수한 점도, 삼투압 특성 보유
- Spray‑dried powder 형태로 높은 용해도 제공

Ficoll™ PM 400
- 진핵 세포 및 세포 소기관 분리에 적합한 배지
- 최대 50%(w/v)의 농도(최대 밀도 1.2 g/mL)로 조제 가능
- 원심 분리 또는 침강 분리용으로 밀도 구배 분리 가능

Xuri™ Cell Expansion System W25
- 세포, 바이러스 및 세포 내 입자의 밀도 구배 원심 분리용 배지
- 저점도·무독성 설계로 세포 생존성 유지
- 최대 1.3 g/mL 범위의 등삼투압 구배 유지
- 사전 형성 또는 중간 속도 원심분리를 통한 자발적 구배 생성 가능

Percoll™ PLUS
- 세포, 세포 내 소기관 및 바이러스 분리에 적합한 배지
- Low endotoxin(< 2 EU/mL)
- 최대 1.3 g/mL 범위의 등삼투압 구배 유지
- 낮은 점도로 낮은 원심력에서 신속한 세포 분리 가능
Cell therapy growth factor
Xuri™ IL-2 growth factor
- T 림프구 활성화 및 증식을 위한 IL‑2 배양 인자
- 파우더 또는 액체 시린지 타입으로 제공
- 검증화된 최적화 프로토콜 및 Regulatory Support File 제공
- USP <1043> 규정 준수
Xuri™ IL-15 growth factor
- Human blood lymphocyte 활성화 및증식을 위한 IL‑15 배양 인자
- 프로세스 표준화 및 공정 개발 기간 단축 지원
- Lot별 생물학적 활성 데이터 제공
- USP <1043> 규전 준수

Xuri™ IL-21 growth factor
- 인간 NK 및 cytotoxic T cell 활성화·증식을 위한 IL‑21 배양 인자
- 프로세스 표준화 및 공정 개발 기간 단축 지원
- Lot별 생물학적 활성 데이터 제공
- USP <1043> 규정 준수
Control Software

Chronicle™ automation software
- 제조 운영 및 공급망을 아우르는 통합 디지털 플랫폼
- eBR·eSOP 기반 GMP 제조 공정 자동화
- Third‑party 장비 포함 데이터 연결 및 공정 추적성 확보
- GAMP 5 · 21 CFR Part 11 · EU Annex 11 지원
Chronicle™ Viewer software
- On‑premises 기반 Cytiva cell therapy 장비 데이터 중앙 관리
- 자동 데이터 수집을 통한 GMP 대응 및 공정 단순화
- GAMP 5 및 21 CFR Part 11 독립 감사 검증
- Audit trail 유지된 데이터 접근 및 추출 지원
UNICORN™ 7 control software
- Research부터 cGMP 제조까지 확장 가능한 통합 제어 소프트웨어
- Method 기반 공정 설계·공유·원격 제어 지원
- 중앙화된 데이터 관리 및 강력한 데이터 보안
- 21 CFR Part 11 대응 및 GAMP 5 기반 설계
Service

Cell Therapy Process Development
- Cell therapy 공정 개발 전략 수립
- 연구 단계부터 임상·상업 생산을 고려한 워크플로 설계
- 밀폐형·자동화 기반 공정 구성 및 최적화
- 공정 재현성과 표준화를 고려한 장비·소모품 구성
- 스케일업 및 스케일아웃을 고려한 제조 설계
- 디지털 기반 공정 관리 및 전자 배치 기록(EBR) 연계
- cGMP 대응을 고려한 공정 설계 및 준비 단계 지원
